Adenoidalny rak torbielowaty (ACC) głowy i szyi, choć rzadki, stanowi znaczące wyzwania ze względu na potencjał lokalnego nawrotu i przerzutów. Pomimo tego, że jest ogólnie powolny, ACC często brakuje skutecznych opcji leczenia, szczególnie w przypadkach nawracających lub przerzutowych. Niedawno zespół naukowców pod przewodnictwem dr Yoshihito Kano z udziałem dr Takahiro Naito z Tokyo Medical and Dental University zbadał skuteczność immunoterapii, szczególnie inhibitorów kontrolnych odporności (ICIS) oraz użyteczności kompleksowego profilu genomowego (CGP) Zarządzając tą potężną chorobą. Ich ustalenia, opublikowane w czasopiśmie Medicina, oświetlają potencjalną rolę ICI i znaczenie identyfikacji biomarkerów do spersonalizowanego leczenia w ACC.
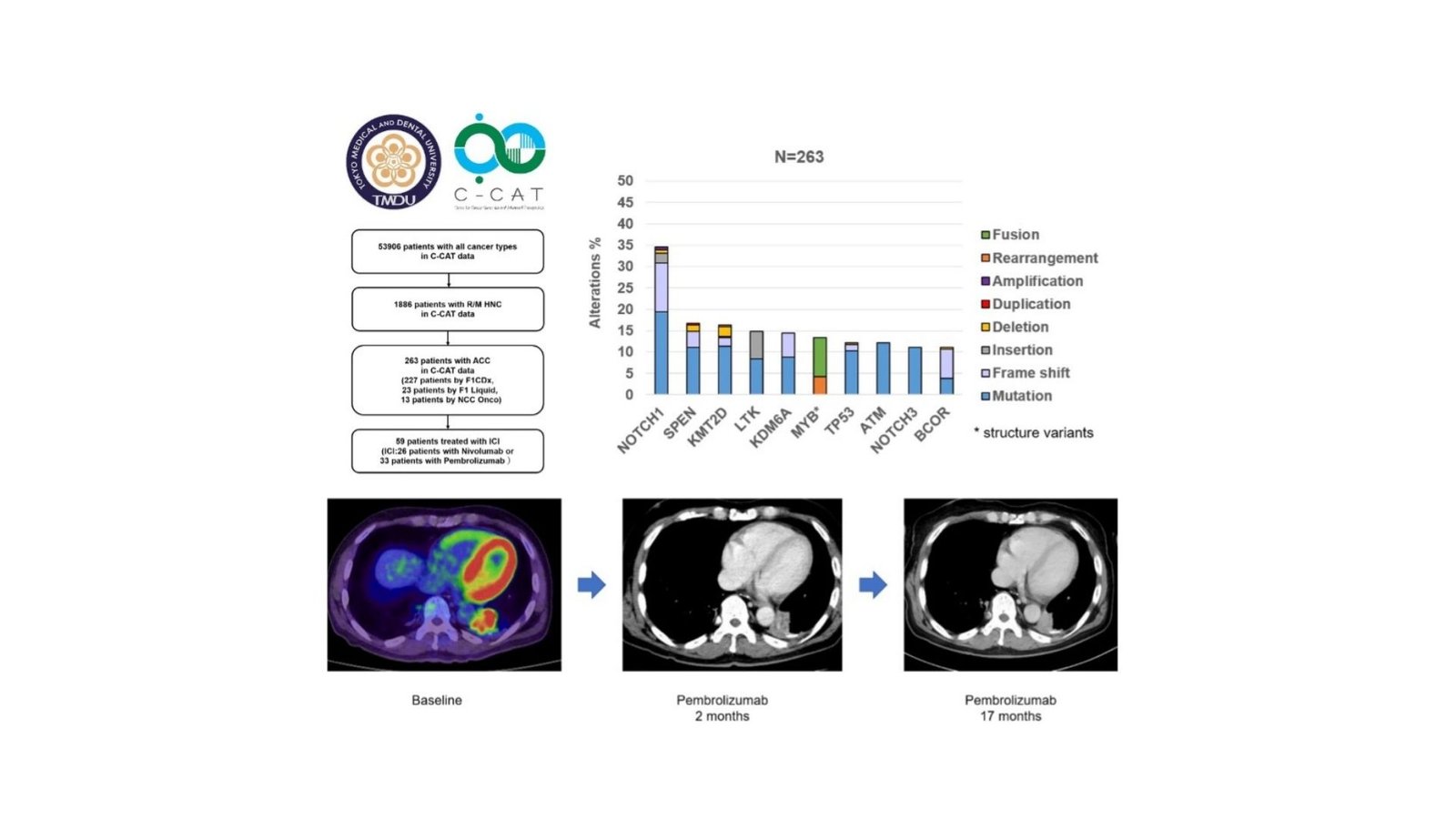
Dr Kano i jego koledzy z TMDU zbadali ogólnokrajową bazę danych zawierającą setki przypadków ACC głowy i szyi. To badanie jest jedną z najobszerniejszych tego rodzaju analiz, oferując wgląd w rzeczywiste zastosowanie ICIS u pacjentów z ACC. Wyniki ujawniły, że chociaż ICI okazały obiecujące, ich skuteczność była ograniczona, z niewielkim obiektywnym wskaźnikiem odpowiedzi (ORR) i około połową pacjentów doświadczających kontroli choroby. Liczby te podkreślają potrzebę wyrafinowanych biomarkerów do przewidywania, którzy pacjenci mogą najbardziej skorzystać z terapii ICI.
Zespół przeanalizował również obciążenie mutacyjne nowotworu (TMB), czynnik często związany z lepszą odpowiedzią na ICI w innych nowotworach. Jednak w przypadku ACC stwierdzono, że TMB jest stosunkowo niski, co może tłumaczyć ograniczoną skuteczność ICI w tej populacji. Co ciekawe, niektórzy pacjenci ze specyficznymi zmianami genetycznymi, takimi jak warianty strukturalne MYB, lepiej reagowali na ICI, sugerując, że warianty te mogą służyć jako potencjalne biomarkery predykcyjne do immunoterapii w ACC.
Dr Kano podkreślił znaczenie tych ustaleń, zauważając: „Nasze badanie podkreśla znaczenie kompleksowego profilowania genomowego w identyfikacji potencjalnych biomarkerów, które mogłyby przewidzieć odpowiedź na immunoterapię u pacjentów z ACC. Podczas gdy ogólna odpowiedź na ICI w ACC jest niewielka, niektóre profile genetyczne, takie jak warianty MYB, mogą oferować szybkość nadziei na bardziej skuteczne strategie leczenia. ”
W swojej szczegółowej analizie naukowcy zidentyfikowali kilka powszechnie zmutowanych genów u pacjentów ACC, w tym NOTCH1, KDM6A i MYB. Wśród nich wariant strukturalny MYB pojawił się jako szczególnie interesujący kandydat do dalszych badań. Badanie wykazało, że pacjenci z wariantami strukturalnymi MYB mieli bardziej korzystną odpowiedź na ICI.
Jeden przypadek, który wyróżnia się 63-letniego pacjenta z guzem gruczołów podżuchwowych, który wykazywał przedłużoną stabilną chorobę po leczeniu pembrolizumabem, ICI. Ten pacjent miał wariant strukturalny MYB wraz z innymi mutacjami, ale udało mu się zachować odpowiedź na terapię przez ponad półtora roku. Ten przypadek podkreśla potencjał MYB jako biomarkera do wyboru pacjentów, którzy mogą skorzystać z immunoterapii.
Badanie wskazało również na wyzwania związane z leczeniem ACC ICI z powodu cech molekularnych i histologicznych guza, takich jak niższa immunogenność i mniej limfocytów infiltrujących guza. Czynniki te przyczyniają się do ograniczonej skuteczności ICI w ACC, pomimo ich sukcesu w innych rodzajach nowotworów głowy i szyi. Niemniej jednak zespół pozostaje optymistą co do przyszłości spersonalizowanej medycyny w leczeniu ACC, opowiadając się za dalszymi badaniami w celu potwierdzenia tych odkryć i zbadania nowych dróg terapeutycznych.
Podsumowując, ta kompleksowa analiza dr Kano i jego zespołu stanowi znaczący krok naprzód w zrozumieniu roli immunoterapii w leczeniu ACC głowy i szyi. Identyfikacja wariantów strukturalnych MYB jako potencjalnego biomarkera oferuje nowy kierunek dla spersonalizowanych strategii leczenia, przynosząc nadzieję pacjentom, którzy mają niewiele opcji. W miarę ewolucji dziedziny medycyny precyzyjnej, takie badania będą miały kluczowe znaczenie w opracowaniu bardziej skutecznego leczenia rzadkich i trudnych nowotworów, takich jak ACC.
Referencje dziennika
Naito, T., Noji, R., Kugimoto, T., Kuroshima, T., Tomioka, H., Fujiwara, S., Suenaga, M., Harada, H., i Kano, Y. (2023). Skuteczność immunoterapii i użyteczności klinicznej kompleksowego profilowania genomowego w torbielowatym raku adenoidalnym głowy i szyi. Medicina, 59, 2111. DOI: https://doi.org/10.3390/medicina59122111
O autorach

Dr Yoshihito Kano jest wybitnym młodszym profesorem nadzwyczajnym na Uniwersytecie Medical and Dental University (TMDU), gdzie specjalizuje się w onkologii medycznej, medycynie genomowej raka i terapii ukierunkowanej. Akademicka podróż dr Kano rozpoczęła się w TMDU, gdzie uzyskał stopień medyczny w 2005 r. Dopierał swoją edukację w tej samej instytucji, kończąc kurs lekarza w oddziale nauk medycznych w 2012 roku.
Oprócz roli w TMDU dr Kano ma imponującą karierę zewnętrzną. Pięć lat spędził jako doktorarzysta na University of Toronto, Department of Laboratory Medicine and Pathobiology, w latach 2014–2019. To międzynarodowe doświadczenie wzbogaciło swoje umiejętności badawcze i kliniczne, szczególnie w biologii genomu, diagnostyce nowotworów i terapeutyce, biologii nowotworów, gastroenterologii, gastroenterologii, gastroenterologii i ogólna medycyna wewnętrzna. Jego wiedza na temat biologii KRAS i ukierunkowanej terapii podkreśla jego znaczący wkład w tę dziedzinę, o czym świadczą jego publikacje w prestiżowych czasopismach, takich jak natury komunikacja, PNAS i badania nad rakiem.
Wkład dr Kano w dziedzinie onkologii podkreśla jego zaangażowanie w rozwój medycyny genomowej raka i rozwijanie ukierunkowanych terapii. Jego praca nadal wpływa na społeczność medyczną, zarówno w Japonii, jak i na arenie międzynarodowej, ponieważ prowadzi innowacyjne badania i zapewnia kompleksową opiekę nad pacjentem.

Dr Takahiro Naito jest dedykowanym dentystą (DDS) specjalizującym się w chirurgii doustnej i szczękowej. Obecnie jest doktorantem na Tokyo Medical and Dental University, Graduate School of Medical and Dental Sciences, koncentrując się na naukach o zdrowiu i inżynierii biomedycznej. Od kwietnia 2021 r. Był aktywnie zaangażowany w kompleksowy projekt analizy genetycznej na temat raka jamy ustnej. Jego badania mają na celu rozwój zrozumienia i leczenia raka jamy ustnej poprzez szczegółowe badania genomowe.